搜索


近日,性直播-粗暴性爱-男女做爱视频 、微生物代谢全国重点实验室邓子新院士团队丁伟课题组和江西师范大学张琪课题组联合在《PNAS》上发表题为“A ribosomally synthesized and posttranslationally modified peptide with ADP-ribosylation”的研究论文。该研究首次发现了一种新型核糖体合成并经翻译后修饰肽(RiPP)天然产物— minviopeptin,并开创性地揭示 ADP-核糖基化可作为RiPP生物合成过程中的内源性关键步骤。研究解析了由自由基SAM酶、ADP-核糖基转移酶和α-酮戊二酸依赖非血红素铁酶协同驱动的全新修饰级联反应,显著拓展了天然产物生物合成的酶学与化学空间。性直播 郭思佳为论文第一作者,丁伟副教授和江西师范大学的张琪教授为共同通讯作者,微生物代谢全国重点实验室为第一通讯单位。
核糖体合成并经翻译后修饰肽是一类重要天然产物家族,以其前体肽基因编码、翻译后修饰多样性、结构复杂及功能丰富等特点,成为天然产物化学与生物合成研究的前沿热点。ADP-核糖基化作为一种广泛的翻译后修饰,在DNA修复、信号转导及细菌毒力调控等中发挥重要作用。然而,在天然产物领域,既往认知中ADP-核糖基化主要与利福霉素的耐药失活相关,从未被证实是天然产物骨架装配本身的组成部分。该研究首次将ADP-核糖基化确立为RiPP生物合成中的构建性修饰,实现了重要的概念创新。
.jpg)
图1. 天然产物中的 ADP-核糖基化。
研究人员通过基因组挖掘,在 Mucilaginibacter inviolabilis 中发现了一个隐蔽的RiPP生物合成基因簇 mic。该基因簇除编码前体肽 MicA 和自由基SAM酶 MicB 外,还编码一个预测的ADP-核糖基转移酶 MicD 以及一个功能未知蛋白 MicC。综合利用异源表达、体外酶学重构、高分辨质谱、核磁共振及晶体结构解析等手段,研究人员系统阐明了该新型天然产物的化学结构、关键酶功能及其完整的生物合成路径。
研究表明,minviopeptin的生物合成遵循严格的“MicB–MicD–MicC”串联修饰级联:MicB首先催化前体肽形成三重交联骨架;随后,MicD在该刚性骨架基础上催化发生ADP-核糖基化修饰;最后,α-酮戊二酸依赖非血红素铁酶MicC催化肽链发生氧化性N–Cα键断裂,生成带有C端酰胺化特征的成熟产物。这一发现揭示了一种前所未有的酶学协作模式。
.jpg)
图2. 在 E. coli 中对 MicB、MicC 和 MicD 的体内功能研究。
进一步结构解析证实,minviopeptin是一种高度修饰的三肽型RiPP,具有三类关键结构特征:特征性交联环骨架、 His5位点的ADP-核糖基化修饰以及 C端酰胺化。 这是首个在结构上得到确证的含ADP-核糖基化修饰的核糖体肽天然产物。
在机制层面,研究人员发现三种修饰之间存在严格的时序依赖性:MicD对底物识别具有严格要求,仅在MicB完成全部三重交联后才可继续催化后续ADP-核糖基化;而MicC则必须要求底物先完成ADP-核糖基化。此外,MicD除利用经典的辅底物 NAD+ 外,对 NADH 也具有一定利用能力,展现了不同于典型ADP-核糖基转移酶的辅底物灵活性。
研究人员还成功解析了MicC的晶体结构。结果显示,MicC具有典型的αKG依赖非血红素铁酶的双链β螺旋折叠特征,并包含保守的 2-His-1-Asp 催化三联体。这一结构基础为深入理解其催化氧化断裂及酰胺化反应的分子机制提供了关键线索,同时也扩展了αKG依赖酶在天然产物生物合成中的已知反应类型。
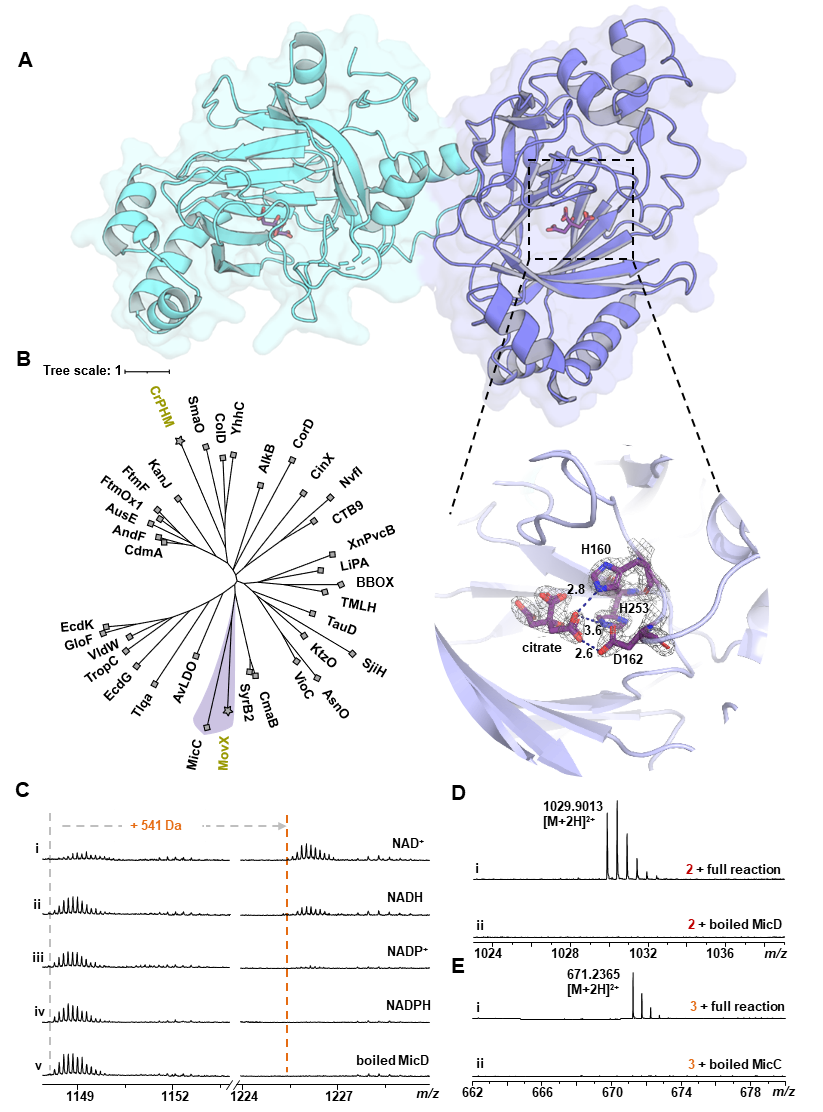
图3. MicC 的结构与系统发育分析,以及 MicD 的底物特异性研究。
该研究不仅发现了一种新型RiPP天然产物,更提出了颠覆性的生物合成新概念:ADP-核糖基化不仅是耐药机制的一部分,更能作为天然产物装配路径中的核心构建步骤。这一成果极大地丰富了核糖体肽天然产物的结构与酶学图谱,为新型
肽类天然产物的挖掘、复杂生物合成机制的解析以及分子工程改造提供了全新的理论基础与研究工具。
研究工作得到了国家重点研发计划(2021YFA0910501)、国家自然科学基金面上项目(22477049和32270070)、联合基金(U22A20451)与中科院西部之光项目(xbzg-zdsys-202105)的资助。
全文链接://www.pnas.org/doi/epdf/10.1073/pnas.2527653123


 性直播
性直播

 性直播概况
性直播概况

 师资队伍
师资队伍

 人才培养
人才培养

 招生就业
招生就业

 科学研究
科学研究

 平台基地
平台基地

 党群工作
党群工作

 校友之家
校友之家

 安全工作
安全工作

 网上办事
网上办事

 当前位置:
当前位置: